Ученые из НИЯУ МИФИ смоделировали молекулы, которые получаются при замещении в фуллерене C20 атомов углерода атомами азота, изучили образование дефектов в соединениях и рассчитали продолжительность их жизни. Статья опубликована в Physica E: Low-dimensional Systems and Nanostructures.
Углерод образует огромное количество аллотропных соединений, обладающих самыми разными свойствами. Особый интерес представляют фуллерены — огромные молекулы, которые содержат от двадцати до нескольких сотен атомов углерода. Впервые фуллерены получили в 1985 году во время наблюдения за парами облучаемого лазером графита, в 1996 году первооткрывателям фуллеренов была присуждена присуждена Нобелевская премия по химии. Подробнее почитать про «обличия» углерода, в том числе про фуллерены, можно в нашей статье.
Помимо «чистых» фуллеренов, состоящих только из атомов углерода, ученые изучают и более сложные соединения, в которых углерод оказывается заменен атомами других химических элементов. Особенно удобно использовать в качестве замены атомы с близкими массами и свойствами, например, азот или бор. Так, длина связей в чистых фуллеренах практически совпадает с расстоянием между атомами углерода и азота в триметиламине, что позволяет атомам азота замещать атомы углерода без существенных изменений структуры фуллерена. В то же время, такое замещение сказывается на электронных и химических свойствах материала. Предполагается, что подобные материалы найдут применение во многих наноэлектронных приборах.
Простейшим фуллереном является молекула C20, в которой атомы углерода выстроены в вершинах икосаэдра. Известно, что при комнатной температуре время жизни этой молекулы очень велико (так что его можно считать бесконечным), а образование в ней дефектов было хорошо изучено в рамках полуэмпирической молекулярной динамики и вычислений «из первых принципов». Тем не менее, замещение отдельных атомов углерода атомами азота может привести к существенному изменению свойств соединений. И хотя системы C20−nNn сейчас тоже активно изучаются, образование дефектов в них еще не исследовалась.
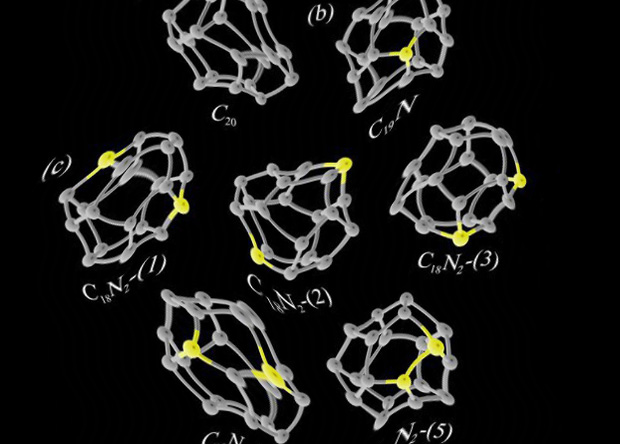
В новой статье ученые Константин Катин и Михаил Маслов исследовали свойства таких соединений фуллерена C20, в которых от одного до трех атомов углерода были заменены на атомы азота. Для этого они численно смоделировали различные соединения и нашли конфигурации с минимальной энергией с помощью программы TeraChem, которая опирается на теорию функционала плотности (DFT). При этом стоит учесть, что свойства соединений C18N2 и C17N3 зависят не только от молекулярного состава, но и от конфигурации (поскольку для них существует несколько изомеров). Свойства изомеров C18N2 ученые изучили по отдельности, а для C17N3 они рассмотрели только одну конфигурацию, в которой атомы азота находятся на максимальном отдалении друг от друга (смотри рисунок).
Для начала исследователи рассчитали, как замещение углерода азотом сказывается на свойствах фуллерена, например, на энергетический зазор между сильно и слабо заполненными электронными оболочками (так называемый HOMO-LUMO gap). Оказалось, что в изомерах C18N2 этот зазор немного больше, чем в чистом C20, а в соединениях C19N и C17N3 он, наоборот, в несколько раз меньше.
Затем химики изучили процесс образования дефектов в подобных соединениях. Согласно с предыдущими теоретическими исследованиями, наименьшую энергию активации в таких соединениях имеют дефекты Стоуна-Уэйлса, которые могут быть рассмотрены как поворот связи углерод—углерод вокруг своего центра на 90 градусов. Оказалось, что у соединений с азотом энергия активации значительно меньше, чем у чистого фуллерена. Так, для C19N она составила примерно 2,98 электронвольт, для различных изомеров C18N2 — от 3,51 до 2,21 электронвольт, а для C20 — 4,93 электронвольт. Такое падение энергии, скорее всего, вызвано тем, что в первую очередь в подобных соединениях разрушается связь между атомами азота и углерода.
Наконец, ученые пересчитали эти значения энергии во время жизни молекул, используя закон Аррениуса. При комнатной температуре падение энергии активации при замещении атомов углерода атомами азота несущественно: время жизни молекул уменьшается, но остается достаточно большим, чтобы его можно было положить бесконечности. Например, время жизни C20 примерно равно 1067 секунд, а C17N3 — 1021 секунд. Другими словами, при комнатной температуре все исследованные соединения остаются стабильными. Однако при больших температурах (порядка 500 градусов Цельсия) эта разница уже более заметна, и хотя чистый фуллерен все так же остается стабильным, молекулы с азотом распадаются (точнее, полимеризуются) за время от одной секунды до нескольких десятков минут.
Кроме того, аналогичным образом ученые смоделировали соединение C19B, в котором замещающим элементом выступает бор, а не азот. Энергия активации в этом случае практически не отличается от энергии для чистого C20 и составляет около 4,47 электронвольт. Это значит, что замещение атомов углерода на атомы бора слабо влияет на свойства соединений (в частности, на время жизни).
Теория функционала плотности часто применяется учеными для численного исследования свойств различных молекул. Например, с помощью этой теории Китайские химики рассчитали параметры соединения углерода и скандия, похожего на фуллерен и напоминающего волейбольный мяч. А Бельгийские исследователи показали, что хотя фуллерен C50 удовлетворяет критерию суперароматичности, он таковым не является.
По информации https://nplus1.ru/news/2018/01/16/MEPhI-fullerene
�