X
ю
ТЗ.), либо вследствие развития в среде разветвл╦нной цепной реакции (цошюй В.).
Тс п лоно и В. осуществляется в условиях, когда тсрмич. равновесие между реагирующим веществом и окружающей! средой окапывается невозможным. При достаточно больших г-шачениях энергии активации £ (истинной или эффективной) скорость хим. реакции w быстро возрастает с увеличением тсмп-ры Т ≈ но закону Аррониуса w~ sexp( ≈ SlRT], R ≈ универсальная газовая постоянная, z ≈ пред экспоненциальный множитель (см. Кинетика химическая] , Т.о. растет и скорость томлоныделсния Q+ в объ╦ме вещества Т';
Цепной В, осуществляется в системах, в к-рых развиваются разветвл╦нный цепные реакции, В процессе таких реакций возникают активные частицы ≈ атомы или радикалы, ведущие реакцию. В простейшем случае скорость изменения концентрации п радикалов описывается ур-нием
(q ≈ тепловой эффект реакции). Темлоотнод во внеш. среду <?_ ≈ через поверхность S зависит от тсмп-ры гораздо слабее:
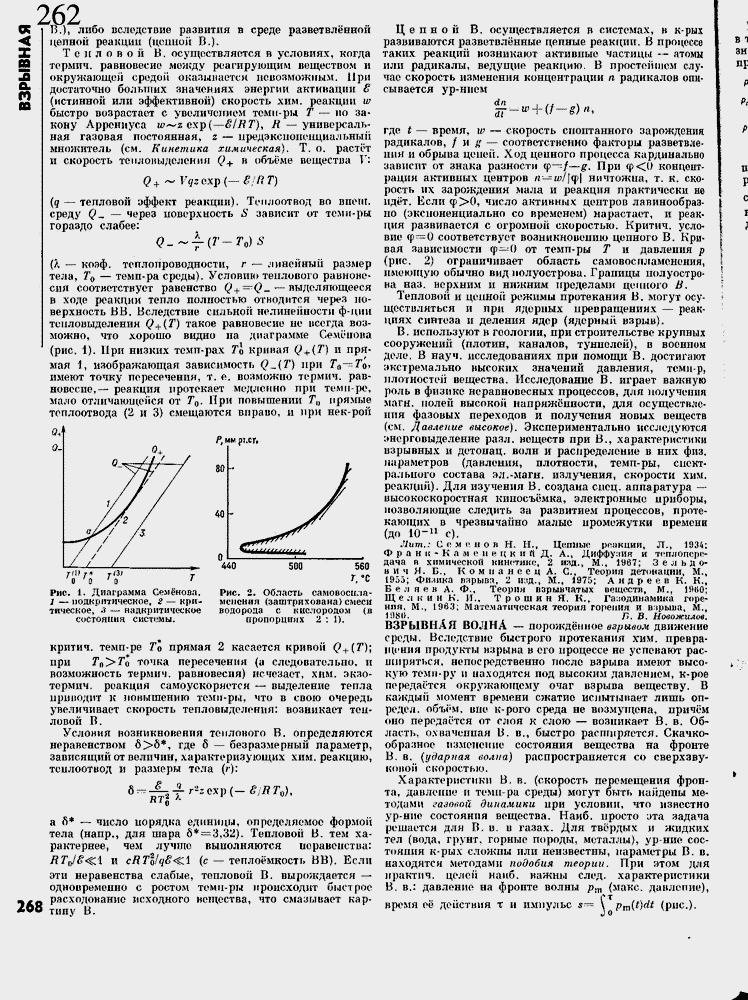
(А ≈ коэф, теплопроводности, г ≈ линейный размер тела, Т$ ≈ темп-pa среды). Условию теплового равновесия соответствует равенство Q + =Q_ ≈ выделяющееся в ходе реакции тепло полностью отводится через поверхность ВВ. Вследствие сильной нелинейности ф-ции тепловыделения Q+(T) такое равновесие не всегда возможно, что хорошо видно па диаграмме Сем╦нова (рис. 1). При низких темп-pax То кривая Q + (T) и пря-
мая 1, изображающая зависимость Q^.(T) при Тп≈Гъ, имеют точку пересечения, т. е. возможно тсрмич. равновесие, ≈ реакция протекает медленно при тем к- ре, мало отличающейся от Т0. При повышении Тп прямые теплоотвода (2 и 3} смещаются вправо, и при нек-рой
0-
Pt мм рт.сг»
80
тшг* Tw ,
ODD '
Рис. 1. Диаграмма Сем╦нова. 1 ≈ иодкритичесное, 2 ≈ критическое, ∙? ≈ надкритическое состояния системы.
440
500
560 Г. "С
Рис. 2. Область самовоспламенения (заштрихована) смеси водорода с кислородом (в пропорциях 2 : 1).
кршич, темп-ре Т0 прямая 2 касается кривой Q+(T);
при Тп^>То точка пересечения (а следовательно, и возможность термич. равновесия) исчезает, хим. экзо-термич. реакция само ускоряете я ≈ выделение тепла приводит к повышению тсмл-ры, что в свою очередь увеличивает скорость тепловыделения: возникает тон-ловой В.
Условия возникновения теплового В. определяются неравенством 6>6*, где б ≈ безразмерный параметр, зависящий от величин, характеризующих хим. реакцию» тешюотвод и размеры тела (г):
268
а и* ≈ число iio рядка единицы, определяемое формой тела (напр., для шара б* ≈ 3,32), Тепловой В. тем характернее, чем лучше выполняются неравенства:
Л7У£<1 и cRTl!q£<£l (с ≈ тепло╦мкость ВВ). Если
эти неравенства слабые, тепловой В. вырождается ≈ одновременно с ростом теми-ры происходит быстрое расходование исходного вещества, что смазывает картину В .
где t ≈ время, w ≈ скорость спонтанного зарождения радикалов, / и g ≈ соответственно факторы разветвления и обрыва цепей. Ход ценного процесса кардинально зависит от знака разности tp≈ / ≈ g. При ф<() концентрация активных центров п≈ ш/|ф| ничтожна, т. к, скорость их зарождения мала и реакция практически не ид╦т. Если <р>0, число активных центров лавинообразно (экспоненциально со временем) нарастает, и реакция развивается с огромной скоростью, Критич, условие ф=0 соответствует возникновению цепного В. Кривая зависимости <р ≈ 0 от темп-ры Т и давления р (рис. 2) ограничивает область самовоспламенения, имеющую обычно вид полуострова. Границы полуострова наз. верхним и нижним пределами цепного В.
Тепловой и цепной режимы протекания В. могут осуществляться и при ядерных превращениях ≈ реакциях синтеза и деления ядер (ядерный взрыв).
В. используют н геологии, при строительстве крупных сооружений (плотин, каналов, туннелей), в военном деле. В науч. исследованиях при помощи В. достигают экстремально высоких значений давления, томи-р, плотностей вещества. Исследование В. играет важную роль в физике неравновесных процессов, для получения магн. нолей высокой напряженности, для осуществления фазовых переходов и получения новых веществ (см, Давление высокое]. Экспериментально исследуются ннсргооыделение разл. веществ при В., характеристики взрывных и детонац. волн и распределение в них физ. параметров (давления, плотности, темп-ры, спектрального состава эл.-магн. излучения, скорости хим. реакций). Для изучения В. создана спец. аппаратура ≈ высокоскоростная киносъемка, электронные приборы, позволяющие следить за развитием процессов, протекающих в чрезвычайно малые промежутки времени (до Ю-11 с).
Лит.: Семенов Н. П., Ценные реакции, Л., 1934; Ф р а н it - К а м е н е ц к и и Д. А., Диффузия и теплопередача в химической кинетике, 2 ияд., М., 1967; 3 е л ь д о-н и ч Я. Б., К о м п а н е е ц А. С., Теория детонации, М., 1955; Физика внрыви, 2 изд., М,, 1975; Андреев К. К.,
Беляев А, Ф., Теория озрылчатых веществ, М., Щ е └'Е к и н К. IT., Т р о ш и н Я. К,, Газодинамика горения, М., 1963; Математическая теория горения и вгфьша, М,, 1П80. Л. В. Новожилов. ВЗРЫВНАЯ ВОЛНА ≈ порожд╦нное взрывом движение среды. Вследствие быстрого протекания хим. превращения продукты нзрына к его процессе не успевают расширяться, непосредственно после взрыва имеют высокую темл-ру и находятся под высоким давлением, к-рое переда╦тся окружающему очаг взрыва веществу. В каждый момент времени сжатие иснытынает лишь оп-редел. объ╦м, вне к-рого среда не возмущена, прич╦м оно переда╦тся от слоя к слою ≈ возникает В. в. Область, охваченная В. в., быстро расширяется. Скачкообразное изменение состояния вещества на фронте В. в. {ударная волна) распространяется со сверхзвуковой скоростью.
Характеристики В. в. (скорость перемещения фронта, давление и темп-pa среды) могут бытт» найдены методами газовой динамики при условии, что известно ур-нпе состояния вещества. Наиб, просто зта задача решается для В. и. в газах. Для тв╦рдых и жидких тел (вода, грунт, горные породы, металлы), ур-ние состояния к-рых сложны или неизвестны, параметры В. в. находятся методами подобия теории. При атом для ирактич. целей наиб, важны след, характеристики В, в.: давление на фронте волны рт (макс, давление),
.... f т время ее действия г и импульс s≈ \\
V "
pm(t)dt (рис.).
")
}


