эВ
О
-0,28
-0,33
-0,54
-0,85
-T,5I
-3.40 -е
В теории атома Сора (см. Атомная физика) радиус простей того А.≈ А, водорода ≈ имеет точно олредел. значение и равняется радиусу наименьшей возможной круговой орбиты: я«0.53-10~* см (точнее, 0.52917х XlO~tf см). Эта величина оказывается удобной естеств. единицей для измерения линейных размеров (с.м, Ес-тествен-пые системы единиц).
Линейные размеры атомных ядер много меньше линейных размеров A. (~l()-1:i ≈К)-12 см), поэтому ядро часто рассматривают как точечный заряд и лишь для топких эффектов взаимодействия ядра с электронными оболочками учитывают его коночные размеры.
Масса А. определяется в осн. массой ого ядра п возрастает пропорционально массовому числу Л,т. е. обще м у ч 11 с л у п р о т о н о в i с нейтронов ≈ числу нуклонов в ядре (ядро содержит Z иротонон и А ≈ Z нейтронов). Масса электрона (0,91-10~а7 г) примерно и 1840 pa;i меньше массы протона или нейтрона (1.67-Ю-21 г), поэтому центр тяжести А. практически совпадает с ядром и можно приближ╦нно считать, что в системе координат, связанной с Л., движутся только электроны, а ядро покоится. Уч╦т движения ядра относительно общего центра тяжести ядра и электронов приводит в теории А. лишь к малым поправкам {см. Изотопический сдви.'^).
Обычно массу А. М выражают к атомных единицах массы (относит, масса А., см. Ат,омная масса). Наиб, точные значения М получаются методами масс-спектроскопии.
Масса Л. не равна в точности сумме масс ядра п электронов, а меньше е╦ па величину дефекта масс, дефект масс для л╦гких А. значительно мены по массы электрона, раст╦т с увеличением 2, но не превышает массы электрона даже для самых тяж╦лых А.
А характеризуется полной энергией, выделяющейся
при его образовании из ядра и электронов,≈ т. е. зпор-глей связи, равной сумме анергий, необходимых для последовав, отрыва от ядра всех У. электронов. Полная энергия быстро возрастает с увеличением Z. Для тяж╦лых А. она составляет песк. сотен кэВ (напр., для А, урана она и4(Ю юВ).
Внутренняя энергия А.≈ его осн. характеристика. А. является квантовой системой, его внутр. энергия квантуется ≈ принимает дискретный (лреры шили) ряд значений, соответствующих устойчивым, стационарным состояниям А., промежуточные значения эта энергия принимать не может. На схемах уровней энергии возможные значения энергии Л. изображаются горизонтальными линиями, расстояния между к-рымп пропорциональны соответствующим разностям
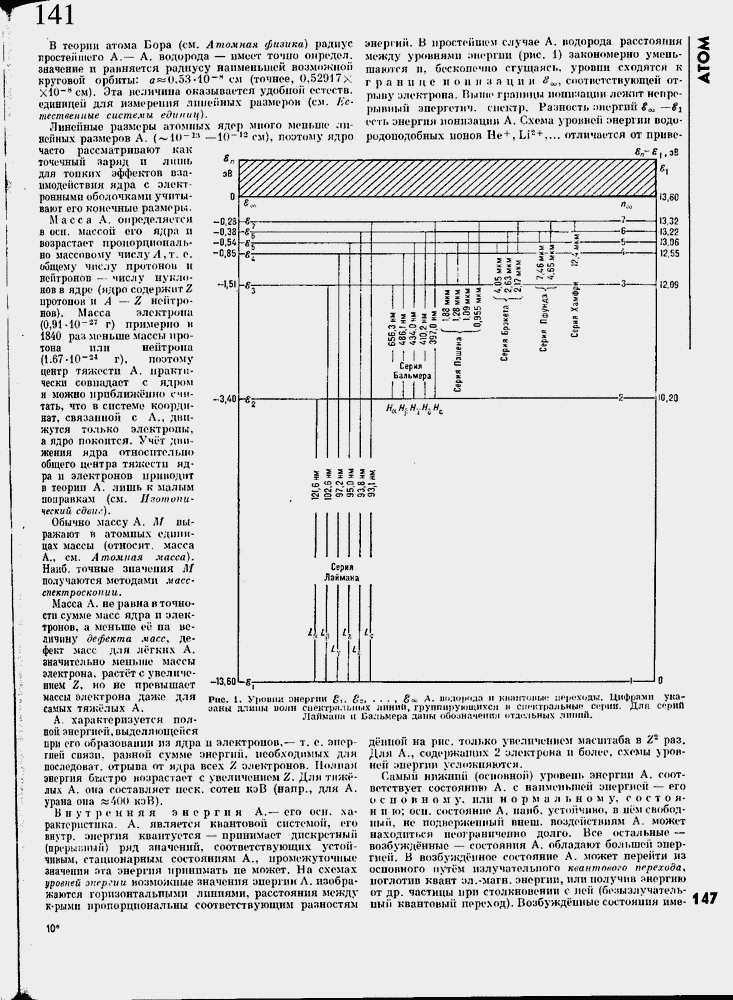
энергии. В простейшем случае А. водорода расстояния между уровнями энергии (рис. 1) закономерно уменьшаются п. бесконечно сгущаясь, уровни сходятся к гран п ц с и о и я з п ц и и #^1 соответствующей отрыву электрона. Вытгк* грпшщы ионизации лежит непрерывный эпергетпч. спектр. Разность энергий £<*, ≈gt есть энергия ионизации А. Схема уровней энергии ооди-родоподобных ионов Не4', Li2 + ,,.. отличается от прнвс-
эВ
Серия Бальмера
*. И,
ем Q ел m CD o>
Серил Лаймана
L
10,20
ка-
I
Рис. 1. Утопии энергии £,, £-, .... S^ A. лпдорода и киннтоиыс пгроходы. Цифрами длины ноли спектральных линий, группирующихся л сш'ктральнып ссфии. Для Лайминм п Бальмера даны иОозначеЕгин отдельных линий,
д╦нпой на рис. тол].ко увеличенном масштаба в Z2 раз. Для А., содержащих 2 электрона, и более, схемы >ровней ЭНерГИИ уСЛ(15КНЯЮТСН.
Самый нижний (основной) уровень энергии А. соответствует состоянию А. с наименьшей энергией ≈ его о с п о к н о м у, или норма л ь н о м у, состоя-н и т; осн. состояние А. наиб, устойчиво, в нем свободный, не подверженный внеш. воздействиям А. может находиться неограниченно долго. Все остальные ≈ возбужд╦нные ≈ состояния А. обладают большей энергией. В возбужденное состояние А. может перейти из основного путем нзлучателыюго квангпокого перехода, поглотив квант эл.-ыагн. энергии, или получив анергию от др. частицы при столкновении с лей (Пе;я,тзлучатель-iibrii квантпвьш переход). Воабужд╦иные состояния име-
о
147
10'
")
}


